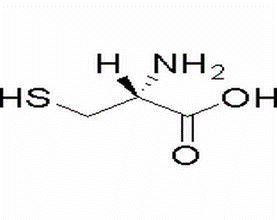
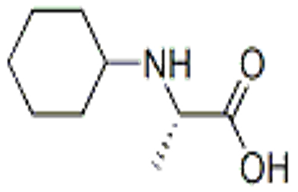ال-سیستئین (CAS# 52-90-4)
| نمادهای خطر | Xn - مضر |
| کدهای ریسک | R22 - در صورت بلعیده شدن مضر است R36/37/38 - تحریک کننده چشم، سیستم تنفسی و پوست. |
| توضیحات ایمنی | S26 – در صورت تماس با چشم، فوراً با آب فراوان بشویید و به پزشک مراجعه کنید. S37/39 - از دستکش مناسب و محافظ چشم/صورت استفاده کنید |
مقدمه
ال سیستئین (L-Cysteine) یک اسید آمینه غیر ضروری است که توسط کدون های UGU و UGC کدگذاری می شود و یک آمینو اسید حاوی سولفیدریل است. به دلیل وجود گروه های سولفیدریل، سمیت آن کم است و به عنوان یک آنتی اکسیدان می تواند از تولید رادیکال های آزاد جلوگیری کند. &&L-سیستئین یک آمینو اسید غیر ضروری است که به طور طبیعی وجود دارد. او فعال کننده NMDA است. همچنین نقش های زیادی در کشت سلول ایفا می کند، به شرح زیر: 1. سوبسترای سنتز پروتئین. گروه سولفیدریل موجود در سیستئین نقش مهمی در تشکیل پیوندهای دی سولفید ایفا می کند و همچنین مسئول تاخوردگی پروتئین ها، تولید ساختارهای ثانویه و سوم است. 2. سنتز استیل کوآ. 3. محافظت از سلول ها در برابر استرس اکسیداتیو. 4. منبع اصلی گوگرد در کشت سلولی است. 5. یونوفور فلزی. و فعالیت بیولوژیکی: سیستئین یک آلفا-آمینه اسید قطبی حاوی گروه های سولفیدریل در گروه آلیفاتیک است. سیستئین یک آمینو اسید ضروری شرطی و اسید آمینه ساکاروژنیک برای بدن انسان است. می تواند از متیونین (متیونین، یک اسید آمینه ضروری برای بدن انسان) تبدیل شود و می تواند به سیستین تبدیل شود. تجزیه سیستئین به پیروات، سولفید هیدروژن و آمونیاک از طریق عمل دسولفوراز در شرایط بی هوازی یا از طریق ترانس آمیناسیون، محصول میانی بتا مرکاپتوپیروات به پیروات و گوگرد تجزیه می شود. در شرایط اکسیداسیون، پس از اکسید شدن به اسید سولفوره سیستئین، می توان آن را با ترانس آمیناسیون به پیروات و اسید سولفور و با دکربوکسیلاسیون به تورین و تورین تجزیه کرد. علاوه بر این، سیستئین یک ترکیب ناپایدار است که به راحتی اکسیداسیون و کاهش می یابد و با سیستین تبدیل می شود. همچنین می توان آن را با ترکیبات معطر سمی تغلیظ کرد تا اسید مرکاپتوریک را برای سم زدایی سنتز کند. سیستئین یک عامل کاهنده است که می تواند باعث تشکیل گلوتن شود، زمان لازم برای اختلاط و انرژی مورد نیاز برای استفاده دارویی را کاهش دهد. سیستئین با تغییر پیوندهای دی سولفیدی بین مولکول های پروتئین و داخل مولکول های پروتئین، ساختار پروتئین را ضعیف می کند، به طوری که پروتئین کشیده می شود.